近期,广东医科大学刘新光教授和黄功华研究员在衰老领域顶级国际学术期刊《Aging Cell》上发表了题为“Pck1 Deficiency Drives Mitochondrial Dysfunction and Cellular Senescence in Adipocytes”的论文,系统阐述了PCK1介导的代谢重塑在维持脂肪组织线粒体稳态和对抗炎性衰老中的核心调控机制,为预防和治疗衰老相关代谢性疾病提供了重要的理论依据和关键靶点。该论文共同第一作者为广东医科大学2021级博士研究生雷仪婷和省医学免疫与分子诊断重点实验室助理研究员杨萌。论文通讯作者为广东省医学免疫与分子诊断重点实验室、广东医科大学医学技术学院刘新光教授和黄功华研究员。

衰老是每个人都无法逃避的生命进程,而白色脂肪组织(WAT)衰老正是这一进程的“早期预警信号”。随着年龄增长,人体脂肪组织等多器官会逐渐出现慢性低度炎症状态——这种现象被称为“炎性衰老”(Inflammaging),它不仅是内脏脂肪增厚、皮下脂肪萎缩以及代谢变慢的元凶,更是2型糖尿病、心血管疾病等年龄相关疾病的重要诱因。目前,针对衰老标志物的研究已经取得了很大进展,但是机体衰老过程中慢性炎症的调控则是一个悬而未决的重大科学问题之一。据此,研究团队聚焦代谢与细胞衰老的交叉领域,首次发现胞质磷酸烯醇式丙酮酸羧激酶(PCK1)是维持脂肪组织线粒体稳态和对抗炎性衰老的核心调控因子。
随着自然衰老进程,性腺和腹股沟WAT中的PCK1表达水平显著下调。通过构建脂肪组织特异性PCK1敲除小鼠模型发现,PCK1缺失会加速小鼠WAT的炎性衰老表型,并诱发机体代谢紊乱。通过非靶向代谢组学和同位素示踪技术,揭示了一条全新的“代谢——炎症”调控机制:正常细胞中,PCK1的功能是促进TCA循环中间产物通过回补反应(cataplerosis)输出到胞质,参与生物合成。当PCK1缺失时,这一“出口”被堵塞,导致延胡索酸(fumarate)在线粒体内大量堆积。过量的延胡索酸破坏线粒体稳态,引发氧化应激,最终导致线粒体DNA(mtDNA)泄漏到细胞质中。泄漏的mtDNA激活了cGAS/STING先天免疫信号通路,进而形成持续的低度慢性炎症。过表达延胡索酸水合酶(Fh1)可加速代谢堆积的延胡索酸,同样能够显著减轻脂肪细胞的炎性衰老表型。这意味着,针对代谢的小分子激活剂或基因治疗,有望成为延缓代谢衰老、实现健康长寿新策略。本研究不仅阐明了PCK1调控线粒体代谢稳态的分子机制,更为开发靶向脂肪组织衰老的新型治疗策略提供了依据。未来,基于脂肪组织PCK1表达水平的检测可望用于评估个体代谢衰老风险。
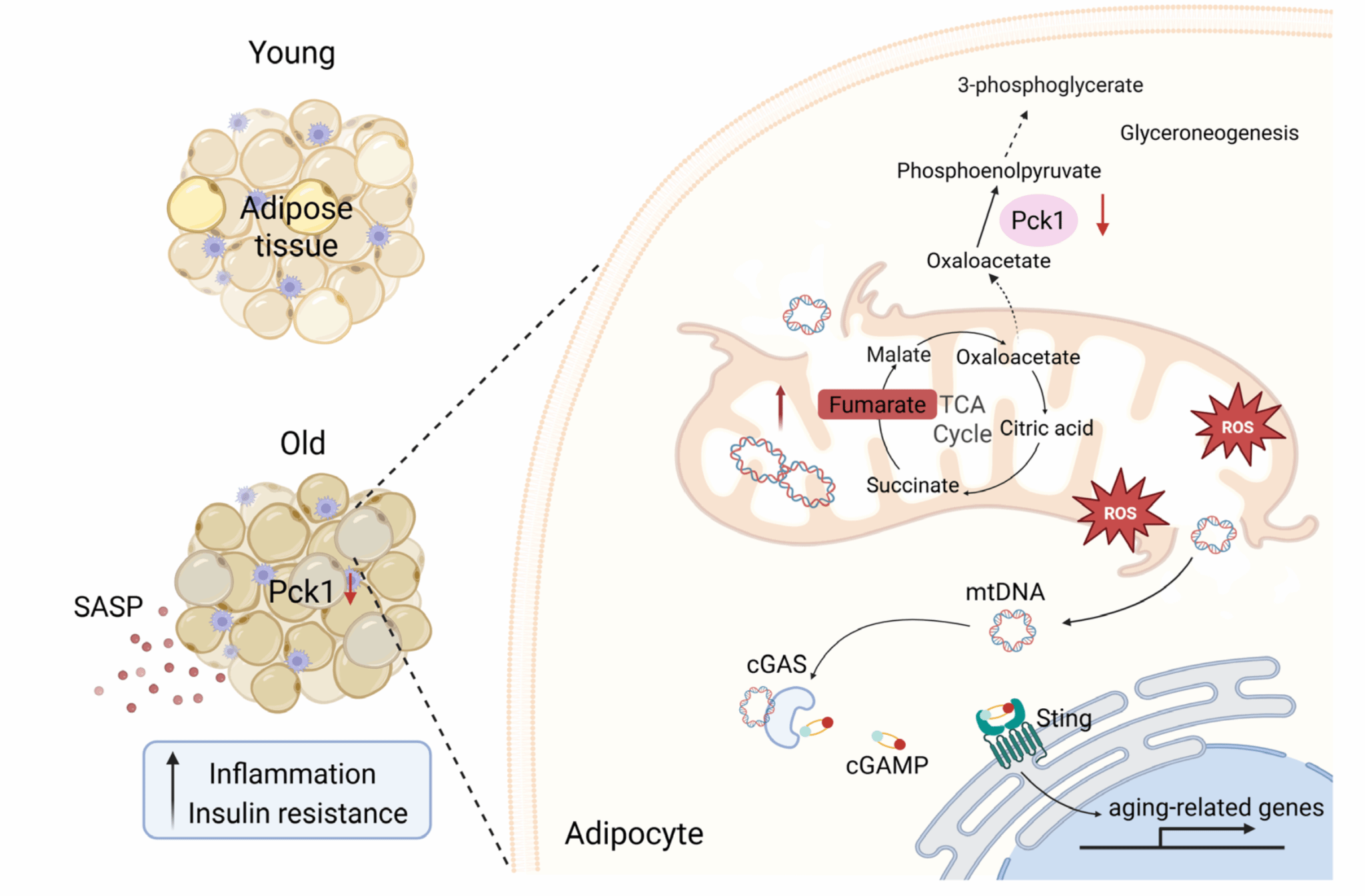
Pck1在脂肪组织衰老中的作用机制图
针对衰老进程中慢性炎症在疾病发生发展中的重要作用,研究团队通过网络药理学与分子对接等实验,从多种天然化合物中筛选出具有较强抗炎抗衰老的小分子,其中穿心莲内酯可明显缓解代谢紊乱所致肾小管上皮细胞炎性衰老引起的肾纤维化(Biochemical Pharmacology, 2024);18β-甘草次酸通过激活SIRT1-TFEB信号减缓代谢紊乱过程中脂毒性诱导的细胞炎性衰老(Phytomedicine, 2025);而穿心莲内酯则通过抑制小胶质细胞中STAT3信号减轻其炎性衰老并改善阿尔茨海默症小鼠的认知和行为学障碍(iScience, accepted in principle)。这些研究为衰老引发慢性炎症及衰老相关疾病的干预提供了直接实验依据。
上述系列研究得到了国家自然科学基金专项项目、面上项目和青年项目,广东省基础与应用基础研究基金粤港澳团队项目等资助。
原文链接:https://onlinelibrary.wiley.com/doi/epdf/10.1111/acel.70462
(图文/杨萌 雷仪婷 审核/韩翠芳 复核/覃继恒 审发/黄功华)